L’essentiel à retenir : la stratégie 2025 transforme la gestion du risque infectieux en passant de la simple surveillance au pilotage prédictif. Grâce à l’intelligence artificielle et aux modèles virtuels utilisés par les CPias et CRAtb, les établissements anticipent désormais les crises. Cette évolution permet de tester l’efficacité des protocoles sanitaires sans aucun risque pour les patients, garantissant une sécurité optimale.
Face à la menace persistante de l’antibiorésistance, comment les établissements de santé peuvent-ils anticiper efficacement les crises sanitaires avant qu’elles ne saturent les services ? La modélisation risque infectieux 2025 apporte une réponse pragmatique en déployant des outils mathématiques avancés pour transformer l’incertitude biologique en stratégie de pilotage opérationnelle. Cette analyse présente comment l’intégration de l’intelligence artificielle et des simulations comportementales permet désormais de sécuriser les décisions médicales et d’optimiser durablement la prévention des infections.
- Le cadre stratégique de 2025 : plus qu’un plan, une boîte à outils
- Les outils opérationnels sur le terrain : CPias et CRAtb en première ligne
- Au-delà de la surveillance : les modèles prédictifs de 2025
- Des modèles virtuels aux applications concrètes à l’hôpital
Le cadre stratégique de 2025 : plus qu’un plan, une boîte à outils
Oubliez les rapports administratifs poussiéreux qui finissent sur une étagère. En 2025, le cadre qui régit la modélisation du risque infectieux n’est pas une théorie bureaucratique, c’est un arsenal tactique. Nous opérons sous l’égide de la Stratégie Nationale de Prévention des Infections et de l’Antibiorésistance, techniquement prévue pour 2022-2025 mais dont la portée a été pragmatiquement étendue. Pourquoi est-ce vital pour vos modèles ? Parce que ce document définit les contraintes physiques de nos simulations. Il impose les variables : flux d’antibiotiques, taux d’observance de l’hygiène et seuils de résistance. Il nous force à passer de la simple observation à l’anticipation active.
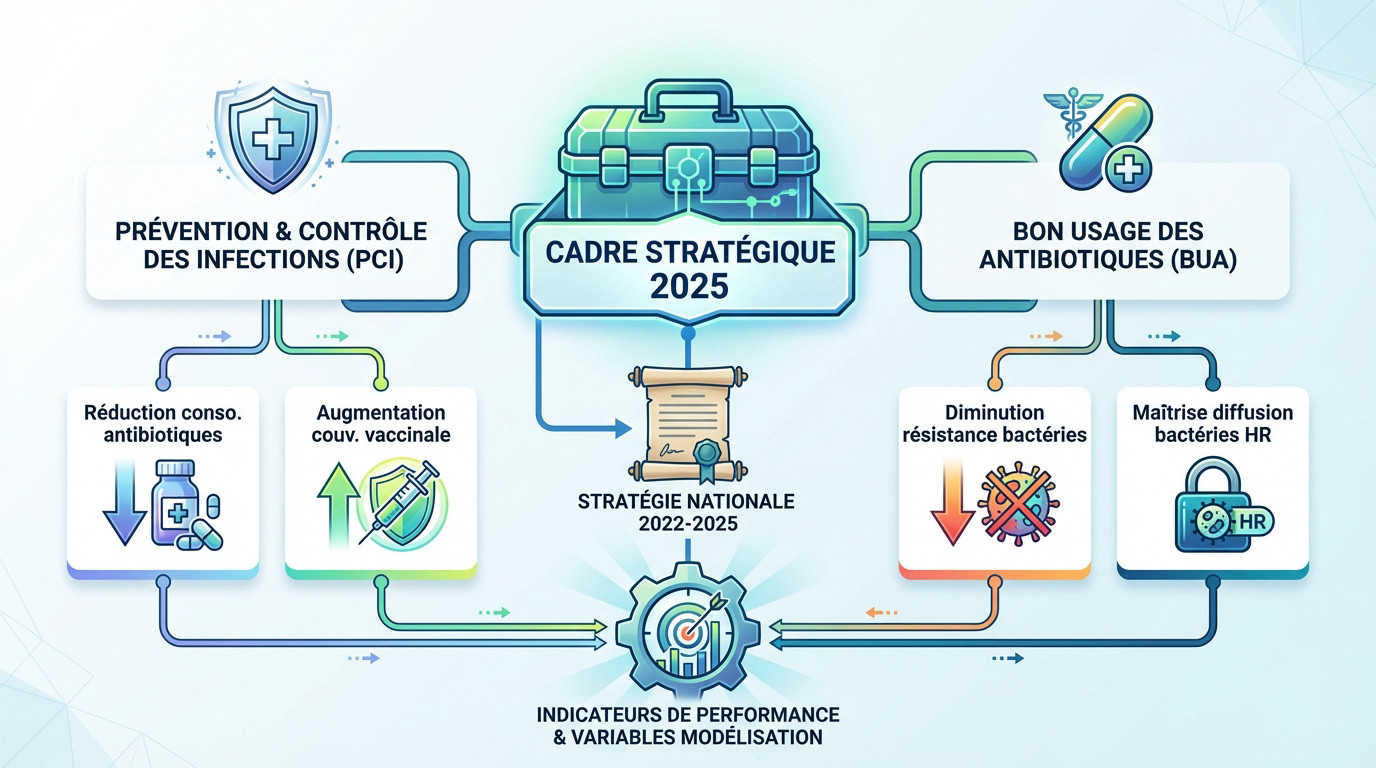
Si vous ignorez ce cadre, vos modèles ne sont que des abstractions mathématiques déconnectées de la réalité terrain. L’enjeu est palpable : 5 500 décès sont attribués chaque année aux bactéries multi-résistantes. Cette stratégie transforme ces statistiques alarmantes en paramètres actionnables. Elle connecte une prescription en ville à une flambée de résistance au CHU. C’est le système d’exploitation sur lequel tournent tous nos outils prédictifs actuels.
La stratégie nationale 2022-2025 comme socle
La modélisation du risque infectieux en 2025 ne sort pas de nulle part. Elle s’inscrit directement dans la feuille de route de la Stratégie Nationale de Prévention des Infections et de l’Antibiorésistance. C’est la base.
Cette stratégie fixe des objectifs clairs et exige des actions concrètes sur le terrain. Elle s’appuie sur deux piliers majeurs : la prévention et le contrôle de l’infection (PCI) et le bon usage des antibiotiques (BUA).
Ne voyez pas ce texte comme un document inerte, mais comme une véritable « boîte à outils » pour les acteurs de terrain. Elle définit les indicateurs et les moyens de pilotage qui alimentent les modèles. C’est le carburant de nos analyses.
Les objectifs chiffrés qui guident la modélisation
Pour modéliser avec précision, il faut des cibles à atteindre. La stratégie 2025 nous fournit ces repères indispensables.
Nos algorithmes intègrent désormais ces contraintes spécifiques :
- Réduction de la consommation d’antibiotiques.
- Augmentation de la couverture vaccinale (grippe, etc.).
- Diminution des taux de résistance pour des bactéries spécifiques.
- Maîtrise de la diffusion des bactéries hautement résistantes.
Ces indicateurs de performance ne sont pas que des chiffres sur un tableau Excel. Ils constituent les variables d’entrée et de sortie centrales des outils de modélisation actuels. Sans eux, l’analyse reste aveugle.
Les outils opérationnels sur le terrain : CPias et CRAtb en première ligne
Le pilotage régional : des données pour agir
Après la stratégie, place au terrain. Les CPias (Centres de Prévention des Infections associées aux soins) et les CRAtb (Centres Régionaux en Antibiothérapie) opèrent comme les relais opérationnels directs des ARS.
Leur rôle ne se limite pas à regarder les chiffres. Ils collectent et analysent les données brutes pour fournir des renseignements exploitables aux établissements de santé. C’est le premier niveau concret de la modélisation.
Cette organisation permet d’agir vite. On s’appuie ici sur des indicateurs qualité en hygiène précis pour ajuster le tir. La réponse devient alors immédiate.
La véritable force de ces centres réside dans leur capacité à transformer la surveillance passive en pilotage actif du risque, grâce à des tableaux de bord régionaux quasi en temps réel.
Tableaux de bord et indicateurs : les outils du quotidien
Les experts naviguent grâce à des tableaux de bord d’indicateurs. Ces outils restent indispensables au quotidien.
| Critère | CPias | CRAtb |
|---|---|---|
| Mission principale | Prévention des infections associées aux soins (IAS) | Promotion du bon usage des antibiotiques (BUA) |
| Outils phares | Tableaux de bord sur les taux d’infections nosocomiales | Tableaux de bord de consommation d’antibiotiques |
| Données analysées | Données de surveillance des IAS (site opératoire, etc.) | Données de prescription et de résistance bactérienne |
| Finalité du modèle | Alerter et guider les protocoles d’hygiène | Ajuster les stratégies d’antibiothérapie et maîtriser l’antibiorésistance |
Au-delà de la surveillance : les modèles prédictifs de 2025
L’intelligence artificielle et le machine learning contre l’antibiorésistance
L’intelligence artificielle n’est plus un fantasme de science-fiction en infectiologie. Elle s’impose aujourd’hui comme un outil pragmatique pour analyser des volumes massifs de données, ces macro-données impossibles à traiter manuellement.
Prenons un cas précis. Des techniques de machine learning décryptent désormais des associations génétiques complexes. Une étude récente sur des bactéries comme E. coli révèle ainsi des schémas de multirésistance invisibles à l’œil nu.
Cette anticipation permet de prédire l’émergence de nouvelles résistances. On adapte alors les stratégies thérapeutiques avant même que la situation clinique ne devienne critique pour le patient.
Modèles à base d’agents (abm) : simuler le facteur humain
Les mathématiques traditionnelles ignorent souvent le facteur humain. Les modèles à base d’agents (ABM) comblent cette lacune en simulant des individus, soignants ou patients, avec leurs propres comportements et interactions.
Les travaux de chercheurs comme Laura Temime sur la transmission hospitalière s’appuient sur ces distinctions méthodologiques :
- Modèles compartimentaux (type SIR) : Pour une vision macroscopique de la population (Susceptibles, Infectés, Rétablis).
- Modèles à base d’agents (ABM) : Pour simuler les interactions individuelles et l’hétérogénéité des comportements.
- Modèles mécanistiques : Pour évaluer l’impact direct d’une intervention, comme une pénurie d’antibiotiques.
Ces modèles s’avèrent parfaits pour tester l’efficacité réelle de mesures sanitaires. Ils valident l’impact du respect de l’hygiène des mains ou de l’organisation des flux de patients.
Des modèles virtuels aux applications concrètes à l’hôpital
Avoir des algorithmes puissants sous le capot, c’est bien. Mais concrètement, à quoi servent-ils au pied du lit du patient en 2025 ? On passe ici de la théorie universitaire à la pratique de terrain : voici comment ces simulations changent la donne dans nos services.
Modéliser l’environnement : flux d’air et vecteurs
On focalise trop souvent sur les mains des soignants. C’est une erreur de débutant. Le risque infectieux ne se limite pas au contact humain ; l’environnement joue un rôle sournois, mais clé, dans la chaîne de transmission.
Pour contrer cela, les experts utilisent la dynamique des fluides (CFD) afin de simuler la dispersion des pathogènes aéroportés dans une chambre ou un bloc opératoire. C’est un point central pour la prévention des infections respiratoires en soins intensifs, où la maîtrise des flux d’air protège les plus fragiles.
Prenons un autre exemple frappant : la modélisation spatiale de la diffusion de vecteurs, comme les moustiques, pour anticiper les risques d’arbovirose. Le modèle ArboCarto illustre parfaitement cette approche : https://agritrop.cirad.fr/614301/.
Tester les stratégies avant de les déployer
Le principal avantage de la modélisation réside dans sa capacité à agir comme un « crash test » virtuel. On peut échouer mille fois sur écran, sans aucun risque pour les patients réels.
Simuler l’impact d’une nouvelle politique de nettoyage ou l’effet d’une pénurie d’antibiotiques permet de choisir la meilleure stratégie avec des preuves chiffrées, pas seulement des intuitions.
Il faut se rendre à l’évidence : la modélisation du risque infectieux en 2025 est devenue un outil d’aide à la décision stratégique, indispensable pour une gestion hospitalière moderne et sécurisée.
La modélisation du risque infectieux en 2025 marque un tournant décisif pour la sécurité sanitaire. En conjuguant stratégie nationale et technologies prédictives, elle dote les hôpitaux d’une capacité d’anticipation inédite. Ces outils transforment la gestion des soins, garantissant une protection optimale des patients face aux menaces émergentes.
FAQ
Quel est le cadre stratégique de la modélisation du risque infectieux en 2025 ?
La modélisation s’inscrit directement dans la Stratégie Nationale de Prévention des Infections et de l’Antibiorésistance 2022-2025, dont les actions se prolongent jusqu’en 2027. Ce cadre fixe des objectifs chiffrés, tels que la réduction de la consommation d’antibiotiques et l’amélioration de la couverture vaccinale, qui servent de variables aux modèles actuels.
Cette stratégie fonctionne comme une boîte à outils pour les professionnels de santé. Elle définit les indicateurs de performance nécessaires pour piloter la prévention et le contrôle de l’infection (PCI) ainsi que le bon usage des antibiotiques (BUA) sur l’ensemble du territoire.
Quels rôles jouent les CPias et les CRAtb dans l’analyse des données ?
Les CPias (Centres d’appui pour la prévention des infections associées aux soins) et les CRAtb (Centres régionaux en antibiothérapie) sont les piliers opérationnels du pilotage régional. Ils collectent et analysent les données de surveillance pour fournir des tableaux de bord décisionnels aux établissements de santé.
Leurs missions sont complémentaires pour modéliser le risque :
- Les CPias se concentrent sur la maîtrise des infections associées aux soins (IAS) et les protocoles d’hygiène.
- Les CRAtb analysent les prescriptions pour promouvoir le bon usage des antibiotiques et lutter contre l’antibiorésistance.
Comment l’intelligence artificielle améliore-t-elle la prédiction de l’antibiorésistance ?
L’intelligence artificielle et le machine learning permettent de traiter des volumes massifs de données (macro-données) pour repérer des signaux faibles. Ces technologies identifient des schémas complexes de résistance bactérienne invisibles via les méthodes traditionnelles.
Grâce à ces modèles prédictifs, il est possible d’anticiper l’émergence de souches multirésistantes. Cela permet aux équipes soignantes d’adapter leurs stratégies thérapeutiques de manière proactive, passant ainsi d’une simple surveillance à une véritable anticipation du risque infectieux.
En quoi la modélisation des flux et des comportements sécurise-t-elle l’hôpital ?
Les outils modernes utilisent la dynamique des fluides (CFD) pour simuler les mouvements d’air et la dispersion des pathogènes dans des environnements clos, comme les blocs opératoires ou les chambres de réanimation. Cela est crucial pour prévenir les infections respiratoires.
En complément, les modèles à base d’agents (ABM) intègrent le facteur humain en simulant les interactions et déplacements des soignants et des patients. Ce couplage technologique permet de tester virtuellement l’efficacité des mesures de prévention avant leur application réelle.