L’essentiel à retenir : les bactéries multirésistantes (BMR) résultent d’une sélection naturelle massivement accélérée par l’usage excessif des antibiotiques. Cette adaptation génétique crée des impasses thérapeutiques majeures, rendant les infections difficiles à traiter. Avec une transmission de gènes 800 000 fois plus fréquente que la mutation spontanée, la préservation de l’efficacité des traitements devient une priorité sanitaire absolue.
Face à l’inefficacité croissante des traitements antibiotiques, comprenez-vous réellement comment certains microbes parviennent aujourd’hui à déjouer la médecine moderne ? Ce dossier pédagogique expose l’origine bactéries multirésistantes et les mécanismes génétiques précis qui transforment une simple infection en impasse thérapeutique. Vous découvrirez ici les processus biologiques invisibles et les comportements quotidiens qui accélèrent cette sélection naturelle redoutable.
- BMR : de quoi parle-t-on exactement ?
- La résistance : une histoire de survie et d’adaptation génétique
- Les stratégies de défense des bactéries face aux antibiotiques
- L’usage des antibiotiques, un accélérateur de résistance
- L’environnement : un réservoir et une autoroute pour les BMR
BMR : de quoi parle-t-on exactement ?
Définir la multirésistance : quand une bactérie devient un casse-tête
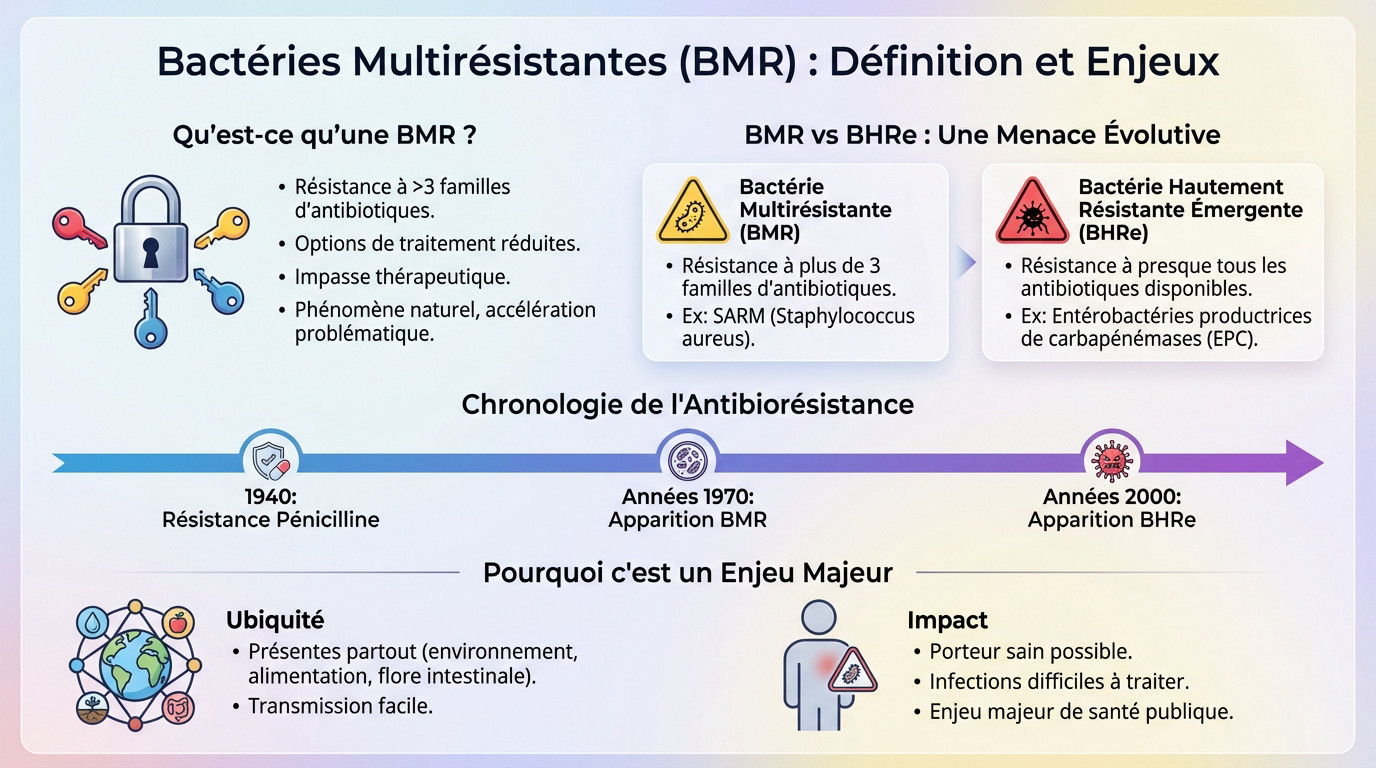
Une bactérie multirésistante (BMR) est un micro-organisme qui a développé une résistance à plus de trois familles d’antibiotiques différentes. Imaginez une serrure de sécurité qui, soudainement, refuse de s’ouvrir avec la majorité des clés habituelles.
La conséquence directe est une réduction drastique des options de traitement pour les médecins. On se retrouve face à une impasse thérapeutique, une situation critique où les infections deviennent extrêmement difficiles, voire impossibles à soigner, mettant la vie du patient en danger.
Si cette résistance est un phénomène naturel d’évolution biologique, son accélération actuelle constitue un problème majeur que nous devons affronter.
BMR, BHRe : une graduation dans la menace
Il faut distinguer les BMR des Bactéries Hautement Résistantes Émergentes (BHRe), qui représentent un niveau de menace supérieur. Ces dernières résistent à la quasi-totalité des antibiotiques disponibles, ne laissant presque aucune arme aux soignants.
Parmi les BMR fréquentes, on trouve le SARM (Staphylococcus aureus résistant à la méticilline). Les BHRe incluent souvent des entérobactéries productrices de carbapénémases (EPC), capables de neutraliser nos antibiotiques de dernier recours.
L’histoire médicale montre une accélération inquiétante : résistance à la pénicilline dès 1940, émergence des BMR dans les années 1970, et apparition des BHRe dans les années 2000, selon les données du Ministère de la Santé.
Pourquoi tout le monde est concerné
Ne pensez pas que les BMR restent confinées à l’hôpital ; elles circulent dans notre environnement, notre alimentation et colonisent notre propre flore intestinale. La transmission se fait aisément, transformant notre microbiome en réservoir potentiel de résistances.
Une personne en parfaite santé peut être porteuse saine sans le savoir. Le danger survient lorsque cette bactérie provoque une infection active, complexe à éradiquer. La multirésistance est aujourd’hui un enjeu majeur de santé publique.
La résistance : une histoire de survie et d’adaptation génétique
Comprendre comment une bactérie apprend à esquiver nos traitements est une question de survie biologique. Ce n’est pas de la malice, c’est simplement de la génétique en action.
Le moteur de l’évolution : la sélection naturelle en action
Voyez l’antibiorésistance comme une sélection darwinienne. L’antibiotique agit tel un prédateur vorace : il élimine les faibles, mais celles possédant une anomalie génétique survivent et se multiplient.
Ce mécanisme de défense est naturel. Des études l’ont montré : on retrouve des traces de bêta-lactamases dans le permafrost datant de 30 000 ans, bien avant la médecine moderne.
Deux chemins pour devenir résistante : mutation ou acquisition
D’abord, la mutation spontanée. C’est un accident génétique rare (1 sur 100 millions) qui modifie la cible de l’antibiotique sur le chromosome, le rendant inefficace.
Ensuite, la voie royale : l’acquisition de gènes. Ici, les bactéries s’échangent des morceaux d’ADN comme des cartes. C’est la transmission horizontale, bien plus redoutable.
Ces gènes voyagent à bord de véhicules spécifiques : les plasmides et les transposons, véritables mini-chromosomes mobiles.
La transmission de gènes via des plasmides est redoutable : elle est 800 000 fois plus fréquente qu’une mutation et peut conférer une résistance à plusieurs antibiotiques d’un seul coup.
Pour visualiser ce déséquilibre, regardez ce comparatif. La différence est effrayante, comme le détaille l’Inserm.
| Mécanisme | Description | Fréquence | Impact |
|---|---|---|---|
| Mutation chromosomique | Modification accidentelle de l’ADN de la bactérie (transmission verticale, de mère à fille). | Rare (environ 1 bactérie sur 100 millions). | La résistance se propage lentement, au fil des générations de la bactérie mutée. |
| Acquisition de gènes | Échange de matériel génétique (plasmides) entre bactéries, même d’espèces différentes (transmission horizontale). | Très fréquente (jusqu’à 1 bactérie sur 100). | Propagation explosive. Une bactérie peut devenir multirésistante instantanément. |
Les stratégies de défense des bactéries face aux antibiotiques
Maintenant que nous savons que les bactéries mutent ou s’échangent des gènes, voyons concrètement quelles sont les « armes » que ces gènes leur fournissent pour contrer les antibiotiques.
Le blindage et l’expulsion : empêcher l’antibiotique d’atteindre sa cible
Imaginez une forteresse qui scelle soudainement ses portes. La bactérie modifie sa membrane externe pour la rendre moins perméable, notamment en altérant ses porines. L’antibiotique ne peut tout simplement plus entrer pour agir. C’est comme renforcer les murs d’un château.
Parfois, l’ennemi réussit quand même à s’infiltrer malgré les murs. La bactérie met en place des « pompes » qui l’expulsent activement vers l’extérieur avant qu’il ne nuise. C’est une défense dynamique et très efficace. Ce rejet mécanique rend le traitement inopérant.
La destruction et le camouflage : neutraliser l’ennemi
Ici, la bactérie passe à l’offensive directe en produisant des enzymes spécifiques. Ces protéines vont « casser » la molécule de l’antibiotique, la rendant inoffensive. Le médicament est détruit avant même d’atteindre son but.
L’exemple le plus connu reste les bêta-lactamases (BLSE), qui détruisent les pénicillines et autres antibiotiques de la même famille. Elles brisent le cycle structurel du médicament. C’est une des causes majeures de résistance.
Enfin, la bactérie peut ruser en changeant sa serrure interne. La bactérie altère la structure sur laquelle l’antibiotique est censé se fixer.
Pour résumer cette guerre microscopique, voici l’arsenal exact déployé :
- Imperméabilité : La bactérie se « verrouille » en modifiant sa paroi pour bloquer l’entrée de l’antibiotique.
- Efflux actif : Des pompes membranaires expulsent l’antibiotique hors de la bactérie dès qu’il pénètre. C’est un système d’éjection permanent.
- Inactivation enzymatique : La bactérie produit des enzymes (comme les BLSE) qui dégradent et neutralisent la molécule d’antibiotique avant qu’elle n’agisse.
- Modification de la cible : La bactérie modifie la structure interne visée par l’antibiotique. L’antibiotique ne peut plus « s’accrocher » et devient inefficace.
La compréhension de ces mécanismes des infections associées aux soins est fondamentale.
L’usage des antibiotiques, un accélérateur de résistance
Ces mécanismes de résistance existent naturellement, mais ils resteraient rares sans un facteur déclenchant : notre propre utilisation des antibiotiques.
La pression de sélection : comment nous favorisons les « super-bactéries »
Imaginez un filtre biologique impitoyable. Chaque fois que l’on utilise un antibiotique, on élimine massivement les bactéries sensibles, mais on laisse involontairement le champ libre aux rares mutantes naturellement blindées. C’est un mécanisme de tri brutal et efficace.
Ces survivantes, désormais débarrassées de toute concurrence, profitent de l’espace vacant pour se multiplier à toute vitesse et devenir la population dominante. Le médicament a littéralement « sélectionné » les souches résistantes.
Le paradoxe, c’est que même un usage médical correct alimente ce mécanisme. Pourtant, c’est bien notre consommation massive et souvent injustifiée qui a fait exploser ce phénomène biologique.
L’erreur humaine : quand « les antibiotiques, c’est pas automatique » prend tout son sens
Nous commettons encore des erreurs grossières en médecine humaine : avaler des antibiotiques pour une simple grippe virale, ne pas finir la boîte ou s’automédiquer avec des restes. Ces pratiques courantes sont un véritable terreau pour la résistance bactérienne.
Vous voyez le piège ? Un traitement trop court ou sous-dosé ne tue pas l’intégralité des pathogènes et « entraîne » simplement les survivantes à devenir plus robustes. C’est la raison précise pour laquelle les antibiotiques ne sont pas automatiques.
Le rôle de l’élevage : un impact souvent sous-estimé
Il faut aussi regarder du côté de l’élevage intensif, qui consomme des quantités astronomiques de médicaments. En réalité, plus de la moitié des antibiotiques produits dans le monde sont destinés aux animaux, selon l’Institut Pasteur.
Même si l’Europe encadre mieux ces pratiques en interdisant les promoteurs de croissance, l’usage reste massif. Cela crée un immense réservoir de bactéries résistantes chez les animaux, prêtes à circuler dans notre environnement.
L’environnement : un réservoir et une autoroute pour les BMR
Le concept « One Health » : une seule santé interconnectée
Oubliez les cloisons étanches entre les espèces. L’approche « One Health » (Une seule santé) démontre que la santé humaine, la santé animale et l’état de notre environnement forment un tout indissociable.
Les bactéries et leurs gènes de résistance voyagent sans passeport entre les humains, les animaux et l’environnement, via l’eau, l’air et la chaîne alimentaire.
Pour comprendre l’origine des bactéries multirésistantes, il faut regarder ce système dans sa globalité. Un bon niveau d’hygiène est directement lié à la lutte contre la résistance bactérienne.
De nos intestins à la rivière : le cycle de la dissémination
Le tube digestif humain et animal constitue le principal réservoir de BMR. Celles-ci sont naturellement excrétées dans les selles avant de se retrouver massivement dans les eaux usées, débutant leur voyage.
Les stations d’épuration filtrent, mais elles ne parviennent pas à éliminer toutes les BMR et leurs gènes. Pire, elles peuvent même devenir des lieux de brassage génétique intense.
Finalement, les BMR sont rejetées dans les rivières et les sols, contaminant durablement l’environnement. D’ailleurs, des études sur les réseaux d’eaux usées le confirment sans équivoque.
L’assiette, un vecteur de transmission silencieux
Voici comment les BMR arrivent dans notre alimentation :
- Contact direct : Les bactéries résistantes issues de l’élevage peuvent contaminer les viandes lors de l’abattage.
- Contamination environnementale : Les fruits et légumes peuvent être contaminés par une eau d’irrigation contenant des BMR.
- Transmission au microbiote : La consommation de ces aliments peut transférer des gènes de résistance à notre propre flore intestinale, même sans causer de maladie immédiate.
La chaîne alimentaire est un vecteur connu de gènes de résistance.
La lutte contre les bactéries multirésistantes nécessite une prise de conscience collective immédiate. L’approche « One Health », liant santé humaine, animale et environnementale, s’avère indispensable pour endiguer ce phénomène. Adoptons un usage responsable des antibiotiques afin de préserver leur efficacité et d’éviter l’impasse thérapeutique.
FAQ
Qu’est-ce qu’une bactérie multirésistante (BMR) exactement ?
Une bactérie multirésistante est un micro-organisme qui a développé des mécanismes de défense contre plusieurs familles d’antibiotiques, généralement plus de trois. Cette accumulation de résistances rend la bactérie insensible aux traitements standards, limitant drastiquement les options thérapeutiques disponibles pour soigner le patient.
Ce phénomène représente une étape critique vers ce que l’on nomme l’impasse thérapeutique. Dans ce cas de figure, les médecins se retrouvent démunis face à une infection qui ne répond plus à aucun antibiotique courant, augmentant ainsi les risques de complications sévères.
Quelle est l’origine biologique de l’antibiorésistance ?
L’antibiorésistance est avant tout un phénomène naturel d’évolution et de survie, comparable à une sélection darwinienne. Les bactéries, présentes sur Terre bien avant l’humanité, possèdent une capacité innée à s’adapter à leur environnement pour survivre aux agressions, y compris celles causées par les substances antibiotiques naturelles.
Cependant, l’utilisation massive d’antibiotiques en médecine humaine et vétérinaire accélère artificiellement ce processus. En éliminant les bactéries sensibles, les traitements laissent le champ libre aux souches résistantes qui se multiplient alors sans concurrence. C’est ce que l’on appelle la pression de sélection.
Pourquoi les bactéries développent-elles des mécanismes de défense aussi rapidement ?
Les bactéries disposent de deux leviers principaux pour devenir résistantes : la mutation génétique spontanée et, surtout, l’acquisition de gènes. La mutation est un « accident » génétique rare qui modifie la structure de la bactérie, la rendant par hasard insensible à un médicament.
L’acquisition est le mécanisme le plus redoutable : les bactéries s’échangent activement des morceaux d’ADN, appelés plasmides, qui contiennent les « plans de construction » de la résistance. Ce transfert horizontal permet à une population bactérienne de devenir multirésistante très rapidement, en récupérant les armes génétiques développées par d’autres.
Quelles sont les bactéries les plus difficiles à traiter actuellement ?
Au-delà des BMR classiques, nous voyons émerger les Bactéries Hautement Résistantes émergentes (BHRe). Ces souches, comme certaines entérobactéries productrices de carbapénémases (EPC) ou les entérocoques résistants aux glycopeptides (ERG), résistent à presque tous les antibiotiques, y compris ceux de dernier recours.
Ces bactéries représentent une menace supérieure car leurs gènes de résistance sont souvent portés par des éléments mobiles très contagieux génétiquement. Elles font l’objet d’une surveillance stricte et de mesures d’isolement spécifiques en milieu hospitalier pour éviter toute propagation épidémique.
Comment une bactérie multirésistante se transmet-elle ?
La transmission des BMR suit les mêmes voies que les bactéries classiques, mais leur persistance rend la situation plus délicate. Elles se propagent principalement par contact direct, via les mains, ou par contact indirect via des surfaces et du matériel contaminés. L’alimentation et l’eau peuvent également servir de vecteurs.
Il faut considérer le concept « Une seule santé » (One Health) : les bactéries circulent librement entre les humains, les animaux d’élevage et l’environnement. Une résistance développée dans un élevage peut ainsi se retrouver chez l’homme via la chaîne alimentaire ou les eaux usées.
Comment agir individuellement pour limiter l’antibiorésistance ?
La lutte contre l’antibiorésistance repose sur un usage raisonné des médicaments. Il est impératif de ne jamais pratiquer l’automédication et de respecter scrupuleusement les doses et la durée des traitements prescrits, même si les symptômes disparaissent avant la fin.
L’hygiène joue également un rôle préventif fondamental. Un lavage des mains fréquent et rigoureux permet de briser la chaîne de transmission des bactéries, qu’elles soient résistantes ou non, limitant ainsi le nombre d’infections et donc la nécessité de recourir aux antibiotiques.