L’essentiel à retenir : Candida auris constitue une menace hospitalière majeure par sa multi-résistance aux traitements, souvent acquise via l’usage intensif de fongicides agricoles. Cette origine environnementale complexifie la protection des patients fragiles, nécessitant une vigilance accrue face à une infection dont le taux de mortalité peut atteindre 70 %.
Comment assurer la sécurité des patients vulnérables lorsqu’un champignon hôpital résistant contamine l’environnement clinique et survit aux désinfectants usuels ? Cette analyse éclaire la relation directe entre les pratiques agricoles intensives et l’apparition de souches fongiques redoutables au cœur de nos services de soins. Vous identifierez ici les failles de notre arsenal thérapeutique actuel et les nouvelles mesures de prévention requises pour maîtriser cette menace silencieuse.
- Candida auris : le nouveau visage de la menace fongique à l’hôpital
- Une résistance qui ne naît pas à l’hôpital
- Face à la menace : entre arsenal limité et failles structurelles
- Comparatif des principaux champignons résistants en milieu hospitalier
Candida auris : le nouveau visage de la menace fongique à l’hôpital
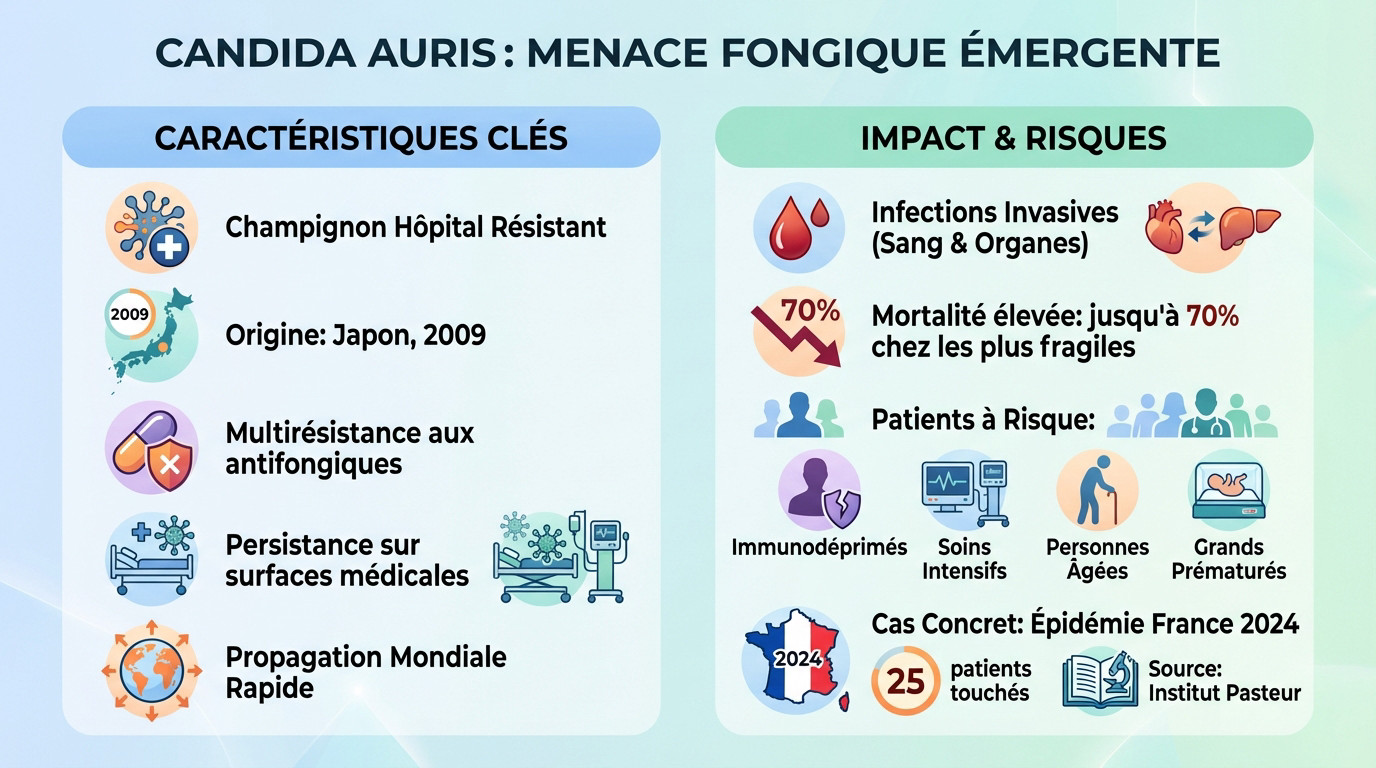
Portrait d’un champignon multirésistant
Identifié au Japon en 2009, Candida auris a franchi les frontières à une vitesse alarmante pour s’installer mondialement. Ce pathogène est aujourd’hui classé comme une priorité absolue de santé publique.
Ce qui inquiète, c’est sa multi-résistance. Il résiste souvent aux trois classes d’antifongiques disponibles, ce qui complique énormément la prise en charge.
De plus, il survit durablement sur le matériel médical. Cette ténacité favorise les types d’infections associées aux soins, car il se propage d’un lit à l’autre en déjouant les nettoyages standards.
Un ennemi redoutable pour les patients vulnérables
Les infections à Candida auris ne sont pas anodines ; elles deviennent invasives en attaquant le sang et les organes. Cette gravité met directement en jeu le pronostic vital des malades.
Les infections invasives à Candida auris sont particulièrement redoutées, avec des taux de mortalité pouvant atteindre 70% chez les patients les plus fragiles, transformant l’hôpital en terrain miné.
Les cibles privilégiées sont les patients vulnérables :
- Les personnes immunodéprimées (chimiothérapie, greffes).
- Les patients en soins intensifs.
- Les personnes âgées et les grands prématurés.
La menace est concrète : une épidémie a touché 25 patients dans un hôpital français en 2024. Ce constat, selon l’Institut Pasteur, confirme une transmission active au cœur de nos établissements.
Une résistance qui ne naît pas à l’hôpital
Mais si ce champignon est un problème hospitalier, son origine est bien plus surprenante. La source de cette résistance se trouve souvent bien loin des couloirs aseptisés.
Quand l’agriculture sélectionne les super-champignons
L’usage massif de fongicides azolés sature nos terres agricoles. Ces produits protègent les récoltes mais partagent une structure chimique quasi identique aux médicaments humains. Les champignons des champs apprennent donc à survivre à ces attaques. Cette accoutumance crée une résistance croisée redoutable.
Prenons le cas concret de l’Aspergillus fumigatus aux Pays-Bas. Sa résistance aux azolés a été tracée jusqu’aux cultures intensives de tulipes. Ce lien prouve que la menace n’est pas confinée aux hôpitaux, mais s’enracine dans les sols.
Une étude sur des pommes en Inde révèle un constat similaire. Les fruits traités abritaient des souches de Candida auris résistantes, absentes sur les fruits frais. L’environnement agricole agit ici comme un véritable incubateur à pathogènes.
L’hôpital, un terrain de jeu idéal
Ces souches endurcies ne restent pas dans les champs. Elles pénètrent les établissements de santé via l’inhalation de spores ou la contamination des surfaces. Le transporteur involontaire est souvent le patient ou le visiteur lui-même.
L’utilisation généralisée des fongicides en agriculture sélectionne des mutants résistants qui, une fois inhalés, peuvent provoquer des infections mortelles chez les patients vulnérables à l’hôpital.
L’hôpital devient le point de rencontre fatal entre des pathogènes déjà armés et une population de patients affaiblis. Ce transfert de résistance rend les traitements classiques inefficaces, un mécanisme confirmé par le CNRS. La sécurité sanitaire dépend désormais de notre gestion agricole.
Face à la menace : entre arsenal limité et failles structurelles
Un combat à armes inégales
La médecine moderne manque cruellement de munitions face à cette guerre microscopique. Pour traiter les infections systémiques graves, nous ne disposons actuellement que de quatre classes de médicaments antifongiques. C’est une vulnérabilité majeure pour la sécurité sanitaire mondiale. En cas de résistance, les options thérapeutiques s’évaporent instantanément.
Voici les piliers de notre défense actuelle, qui s’effritent dangereusement :
- Les polyènes, les azolés, les échinocandines et la flucytosine.
- Le redoutable C. auris résiste souvent à plusieurs d’entre elles simultanément.
- Cette pan-résistance laisse les médecins sans solution viable.
L’absence d’outils de diagnostic rapides reste un frein majeur, surtout dans les pays à faibles revenus. On navigue souvent à l’aveugle face à l’infection. Cela engendre des retards de traitement fatals ou des prescriptions inadaptées.
Les angles morts de l’hygiène hospitalière
Les failles organisationnelles fragilisent nos structures de soins. La pression constante sur le personnel soignant est bien réelle. Elle entraîne parfois une dégradation involontaire du bio-nettoyage. De plus, certains désinfectants utilisés s’avèrent inefficaces contre ces champignons tenaces.
Le danger vient aussi du concept de porteur sain. Un patient peut héberger le champignon sur sa peau sans présenter le moindre symptôme. Il le transmet alors involontairement à des voisins de chambre plus vulnérables. C’est une bombe à retardement invisible pour la maîtrise des épidémies.
La surveillance des pathogènes émergents comme C. auris doit devenir une priorité absolue. Il faut adapter nos stratégies de prévention sans attendre. Le dépistage systématique des porteurs et des protocoles d’hygiène renforcés sont nos seuls remparts.
Comparatif des principaux champignons résistants en milieu hospitalier
Ces deux pathogènes dominent les craintes actuelles en infectiologie. Voici leurs différences fondamentales.
Tableau récapitulatif
Ce comparatif résume l’urgence sanitaire, de la transmission à une létalité qui ne tolère aucune erreur :
| Caractéristique | Candida auris | Aspergillus fumigatus résistant |
|---|---|---|
| Type de champignon | Levure | Moisissure filamenteuse |
| Principal mode de transmission | Contact (surfaces, peau), infection nosocomiale | Inhalation de spores présentes dans l’air |
| Niveau de résistance | Souvent multi-résistant (polyènes, azolés, échinocandines) | Résistance croissante aux azolés |
| Taux de mortalité (infections invasives) | Élevé (jusqu’à 70%) | Élevé (dépasse 50% chez les patients à risque) |
| Origine de la résistance | Liens suspectés avec les fongicides agricoles | Fortement lié à l’usage de fongicides azolés en agriculture |
Face à l’émergence de Candida auris, la vigilance s’impose bien au-delà des murs de l’hôpital. La réduction des risques passe par une révision des pratiques agricoles et un renforcement strict de l’hygiène hospitalière. Seule une stratégie globale, unissant santé humaine et environnementale, permettra de contenir cette menace silencieuse pour les patients fragiles.
FAQ
Quel champignon résistant aux médicaments se propage actuellement dans les hôpitaux ?
Le principal agent pathogène qui préoccupe actuellement les autorités sanitaires est Candida auris. Ce champignon, identifié récemment, se distingue par sa capacité à survivre longtemps sur les surfaces et le matériel médical, facilitant ainsi sa transmission d’un patient à l’autre. Sa particularité réside dans sa multi-résistance fréquente aux principales classes d’antifongiques, ce qui place souvent les médecins dans une impasse thérapeutique.
Les infections fongiques peuvent-elles devenir résistantes aux traitements ?
Oui, les champignons développent des mécanismes de défense similaires à ceux des bactéries face aux antibiotiques. Cette résistance trouve souvent son origine hors de l’hôpital, notamment à cause de l’usage massif de fongicides agricoles. Ces produits, chimiquement proches des médicaments utilisés en médecine humaine, sélectionnent des souches résistantes dans l’environnement (sur des fleurs ou des fruits) qui finissent par infecter les patients vulnérables.
Quels sont les symptômes d’une infection au champignon Candida auris ?
L’identification des symptômes est complexe car Candida auris infecte souvent des patients déjà hospitalisés pour d’autres pathologies graves. Les signes les plus courants sont une fièvre élevée et des frissons qui ne diminuent pas après un traitement antibiotique classique. Seul un test de laboratoire spécifique permet de confirmer la présence de ce champignon, car il peut être confondu avec d’autres levures plus banales.
Est-ce qu’une mycose peut entraîner la mort ?
Si la plupart des mycoses cutanées sont bénignes, les infections fongiques invasives qui touchent le sang ou les organes vitaux sont extrêmement dangereuses. Chez les patients immunodéprimés ou en soins intensifs, le taux de mortalité peut être très élevé. Dans le cas de certaines souches résistantes, ce taux peut atteindre jusqu’à 70 %, transformant une infection opportuniste en une urgence vitale majeure.
Quels sont les principaux types de champignons d’importance médicale ?
En milieu hospitalier, deux grandes catégories de champignons menacent les patients : les levures, comme le genre Candida, et les moisissures filamenteuses, dont le représentant le plus redouté est Aspergillus fumigatus. Ces deux types de pathogènes profitent de l’affaiblissement du système immunitaire pour se développer et présentent aujourd’hui des niveaux de résistance aux traitements de plus en plus préoccupants.
L’amoxicilline est-elle un antifongique ?
Non, l’amoxicilline est un antibiotique conçu pour éliminer les bactéries ; elle n’a aucune efficacité contre les champignons ou les virus. Au contraire, l’utilisation inappropriée d’antibiotiques peut favoriser les infections fongiques en détruisant la flore bactérienne naturelle qui empêche habituellement les champignons de proliférer. Le traitement des mycoses nécessite l’usage de médicaments spécifiques appelés antifongiques.



