L’essentiel à retenir : l’identification des bactéries résistantes repose sur la complémentarité entre l’antibiogramme et les techniques moléculaires ciblant directement l’ADN. Cette stratégie hybride sécurise la prise en charge thérapeutique et limite la transmission, notamment grâce aux tests génétiques rapides qui réduisent le délai de détection de 48 heures à moins d’une heure.
Face à l’incertitude clinique d’une infection qui persiste, la précision et la rapidité du diagnostic biologique déterminent souvent l’issue du parcours de soins pour le patient. Cet article décrypte les protocoles analytiques rigoureux, depuis l’antibiogramme standard jusqu’aux technologies de séquençage ADN, spécifiquement mis en œuvre pour assurer une identification bactéries résistantes fiable au sein des plateaux techniques modernes. Vous découvrirez comment l’expertise du laboratoire permet de cibler précisément les souches pathogènes et d’ajuster les thérapies pour contourner les mécanismes de défense microbiens les plus sophistiqués.
- Avant la résistance, l’identification : qui est l’ennemi ?
- L’approche classique (phénotypique) : observer pour comprendre
- La révolution moléculaire (génotypique) : lire le code de la résistance
- Les outils de l’identification rapide : pcr et technologies émergentes
- Phénotype et génotype : deux approches complémentaires, pas opposées
- Les défis actuels et l’avenir du diagnostic de la résistance
Avant la résistance, l’identification : qui est l’ennemi ?
La première étape : mettre un nom sur le pathogène
Tout commence par un prélèvement, sanguin ou urinaire. Le but initial n’est pas de chercher la résistance, mais d’abord d’identifier la bactérie responsable. C’est le point de départ de toute analyse.
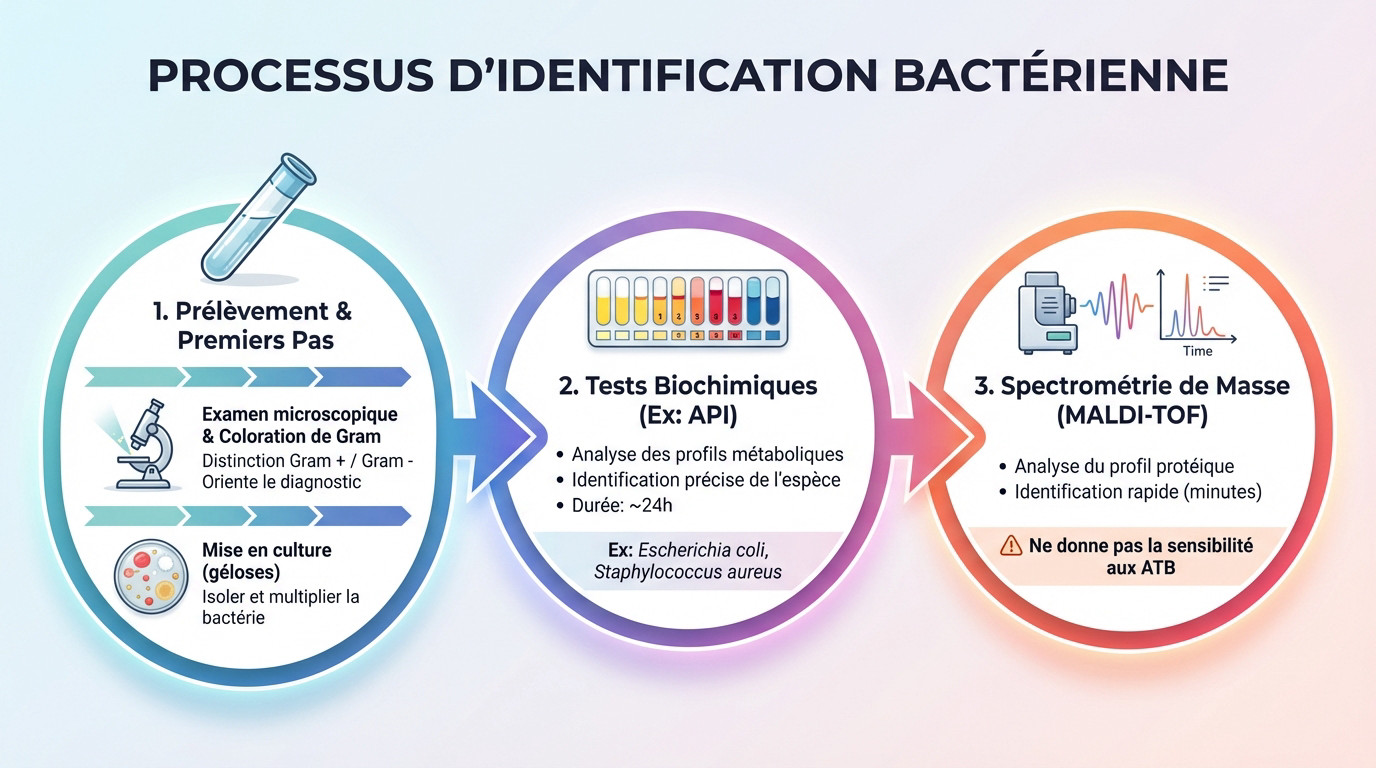
On utilise des méthodes de base : l’examen microscopique après coloration de Gram distingue les grandes familles, Gram positif ou négatif. Cette étape simple oriente déjà le diagnostic et les premières décisions médicales.
La mise en culture sur des géloses spécifiques permet ensuite d’isoler la bactérie en la faisant se multiplier.
Les tests biochimiques : la carte d’identité de la bactérie
Une fois la bactérie isolée, on emploie des galeries de tests biochimiques. Le principe est simple : on observe si la bactérie est capable de « consommer » différents sucres ou de produire certaines enzymes.
Cela établit son « profil métabolique », une véritable signature biologique. Chaque espèce possède des caractéristiques uniques. C’est cette carte d’identité précise qui permet de dire avec une certitude absolue : « c’est un Escherichia coli » ou « un Staphylococcus aureus« .
Ce n’est qu’après cette identification formelle que la question de sa résistance se pose.
L’arrivée de la spectrométrie de masse (MALDI-TOF)
Les laboratoires modernes utilisent de plus en plus la spectrométrie de masse MALDI-TOF. Cette technologie analyse le profil des protéines d’une colonie bactérienne pour l’identifier en quelques minutes. C’est une méthode analytique puissante.
Cette méthode a considérablement accéléré l’étape d’identification par rapport aux tests biochimiques classiques qui demandent souvent 24h. Le gain de temps pour la prise en charge est déjà conséquent.
Cette technique identifie la bactérie, mais ne dit rien sur sa sensibilité aux antibiotiques. C’est l’étape suivante.
L’approche classique (phénotypique) : observer pour comprendre
L’antibiogramme : le test de référence historique
L’antibiogramme constitue la méthode fondamentale pour tester la sensibilité d’une bactérie. Son principe consiste à observer directement si un antibiotique spécifique parvient à empêcher ou non sa croissance.
On utilise souvent la méthode par diffusion en milieu gélosé. Des disques imprégnés d’antibiotiques sont déposés sur une « pelouse » de bactéries cultivées. Si la bactérie est sensible, un « halo » sans culture se forme nettement autour du disque.
La taille précise de ce halo indique le degré de sensibilité. En l’absence de halo visible, la bactérie est alors classée comme résistante.
La concentration minimale inhibitrice (CMI) : une mesure de précision
La CMI s’impose comme une méthode plus quantitative. Le but n’est plus seulement de savoir si la bactérie est résistante, mais de déterminer la plus petite concentration d’antibiotique nécessaire pour l’inhiber. C’est une mesure d’une précision chirurgicale.
Cette analyse passe par la technique de micro-dilution en milieu liquide. La bactérie est mise en présence de concentrations décroissantes d’antibiotique réparties dans de multiples puits. C’est une échelle de dosage.
La CMI correspond au dernier puits où aucune croissance n’est visible. Cette valeur guide le dosage.
Le talon d’Achille de l’approche phénotypique : le temps
Le problème majeur de ces techniques est leur dépendance biologique. Elles dépendent de la vitesse de croissance de la bactérie. Il faut attendre que la bactérie se multiplie pour voir si elle est inhibée.
Il faut chiffrer ce délai technique incompressible. Il faut compter 24 à 72 heures, voire plusieurs semaines pour les bactéries à croissance lente comme celle de la tuberculose. Ce délai est une éternité.
Le décalage temporel pose un risque immédiat pour la survie du malade. L’urgence clinique s’accommode très mal de cette attente.
Attendre deux jours un antibiogramme pour un patient en septicémie, c’est laisser un boulevard à l’infection et potentiellement utiliser un traitement inefficace à l’aveugle.
La révolution moléculaire (génotypique) : lire le code de la résistance
Face à l’urgence, il fallait trouver un moyen de contourner le temps de culture. La solution ? Ne plus observer le comportement de la bactérie, mais aller lire directement dans son ADN les causes de sa résistance.
Changement de paradigme : chercher le gène, pas l’effet
Ici, on change totalement d’approche. Au lieu d’attendre de voir si la bactérie survit à l’antibiotique, on traque la cause racine. On fouille directement son matériel génétique (ADN). L’objectif est de repérer la présence de gènes de résistance connus.
Imaginez la scène. C’est comme vérifier sous le capot si une voiture a un moteur de course (le gène) au lieu d’attendre de la voir rouler sur un circuit (le test phénotypique).
L’avantage est immense : plus besoin d’attendre que la bactérie pousse. L’analyse peut être faite très rapidement.
Les cibles de la biologie moléculaire : gènes et mutations
Ces méthodes ciblent des séquences d’ADN très précises. Elles trahissent la capacité de la bactérie à se défendre. Souvent, ce sont des gènes codant pour des enzymes destructrices d’antibiotiques.
On pense tout de suite aux gènes codant pour les bêta-lactamases (BLSE) ou les carbapénémases.
| Bactérie type | Antibiotique concerné | Gène de résistance recherché |
|---|---|---|
| Staphylococcus aureus | Méticilline | mecA |
| Enterobacteriaceae | Céphalosporines de 3ème génération | Gènes CTX-M (pour les BLSE) |
| Enterobacteriaceae, Pseudomonas aeruginosa | Carbapénèmes | Gènes KPC, NDM-1, OXA-48 |
| Mycobacterium tuberculosis | Rifampicine | Mutations dans le gène rpoB |
| Enterococcus faecium | Vancomycine | Opérons vanA, vanB |
Le gain de temps : l’atout maître du génotypage
La rapidité change tout. On obtient des réponses fiables en quelques heures seulement. Parfois, le verdict tombe en moins d’une heure, directement depuis le prélèvement du patient.
Cette accélération permet de passer de 48 heures à moins d’une heure pour le diagnostic. On instaure immédiatement le bon traitement antibiotique. Les mesures d’isolement sont prises aussitôt. Cela stoppe net la propagation.
Gagner 47 heures sur le diagnostic d’une bactérie multirésistante, ce n’est pas un confort de laboratoire, c’est une chance de survie supplémentaire pour le patient.
Les outils de l’identification rapide : pcr et technologies émergentes
Parler de « lire l’ADN » est une chose, mais concrètement, comment les laboratoires font-ils ? Plusieurs technologies, dominées par la PCR, sont au cœur de cette approche moléculaire.
La PCR : la pierre angulaire du diagnostic moléculaire
La PCR (Polymerase Chain Reaction) s’impose aujourd’hui comme la technique reine au laboratoire. Son principe ressemble à une photocopieuse à ADN ultra-performante. Elle va cibler puis amplifier en millions d’exemplaires un gène de résistance spécifique s’il est présent. C’est le seul moyen de le rendre visible.
Si la machine détecte cette amplification, le verdict tombe immédiatement. La bactérie est donc porteuse du gène de résistance recherché. S’il n’y a pas d’amplification, le gène est tout simplement absent.
Notez que les systèmes de PCR en temps réel (qPCR) donnent un résultat en moins d’une heure. Cela a radicalement transformé la prise en charge des urgences infectieuses.
Les tests rapides immunochromatographiques et colorimétriques
Une autre approche change la donne : les tests immunochromatographiques (ICT). Le fonctionnement rappelle furieusement celui d’un simple test de grossesse. Ils détectent une protéine spécifique de la résistance, comme la PBP2a pour le SARM, directement sur la souche.
D’autres outils, comme les tests colorimétriques développés par l’Inserm, misent sur la chimie visuelle. Ces tests, basés sur un changement de couleur, permettent de détecter l’activité d’enzymes de résistance en moins de deux heures. C’est une efficacité redoutable.
Leur simplicité d’utilisation est déconcertante. Soulignons aussi leur faible coût, qui les rendent très attractifs.
Au-delà de la PCR : puces à ADN et séquençage
Les puces à ADN (microarrays) représentent une évolution logique de la PCR classique. Elles permettent de ne plus chercher un seul coupable, mais de scanner large. On peut ainsi rechercher simultanément des centaines de gènes de résistance différents en une seule analyse.
Mais le séquençage du génome entier (WGS) reste l’approche la plus complète à ce jour. Au lieu de chercher des gènes connus, on décode tout l’ADN de la bactérie. Cela permet de trouver tous les gènes de résistance, même les plus rares ou émergents.
Le séquençage est encore surtout un outil de recherche et de surveillance épidémiologique. Pourtant, il se rapproche chaque jour de la routine clinique.
Phénotype et génotype : deux approches complémentaires, pas opposées
Avec ces technologies moléculaires si rapides, on pourrait penser que le bon vieil antibiogramme est bon pour le musée. En réalité, la situation est plus nuancée et les deux approches cohabitent.
Les limites du « tout génétique »
Le premier écueil du génotypage est simple : on ne trouve que ce que l’on cherche. Un test PCR ne détectera pas un nouveau mécanisme de résistance ou un gène inconnu. C’est un angle mort technologique.
Le second problème réside dans l’expression des gènes : la présence d’un gène ne signifie pas toujours qu’il est actif. Une bactérie peut posséder un gène de résistance mais ne pas l’utiliser, et donc rester sensible à l’antibiotique. Le génotype ne dit pas tout.
C’est une limite majeure : le test génotypique peut parfois surestimer la résistance, ce qui n’est pas sans conséquence sur le choix du traitement.
Pourquoi l’antibiogramme reste indispensable
L’antibiogramme, lui, donne une réponse sans ambiguïté sur le comportement réel de la bactérie. Il teste l’effet final : la bactérie pousse-t-elle, oui ou non ? Il détecte tous les mécanismes de résistance, connus ou inconnus. Rien ne lui échappe.
C’est la seule méthode qui confirme la résistance de manière fonctionnelle. Il reste donc le « gold standard » pour confirmer un résultat et pour tester des antibiotiques pour lesquels il n’existe pas de test moléculaire.
De plus, la mesure de la CMI reste incontournable pour ajuster les posologies.
Vers une stratégie combinée en laboratoire
Voici la stratégie actuelle dans la plupart des laboratoires. En cas d’urgence, comme une septicémie, on lance un test moléculaire rapide pour une orientation immédiate et pour prendre des décisions rapides sur le traitement et l’isolement.
En parallèle, on lance systématiquement une culture et un antibiogramme complet. Ce dernier viendra confirmer, affiner ou corriger le résultat initial 24 à 48h plus tard face à une bactérie multirésistante (BMR), garantissant la meilleure prise en charge possible.
Les défis actuels et l’avenir du diagnostic de la résistance
La surveillance des résistances émergentes
Le vrai danger réside dans l’apparition de nouvelles formes de résistance encore inconnues. Les bactéries évoluent sans cesse, développant des mutations ou acquérant de nouveaux gènes pour survivre aux traitements.
C’est ici qu’interviennent les réseaux de surveillance, comme celui du CDC aux États-Unis. Ces structures collectent les souches bactériennes atypiques pour les analyser et mettent à jour les tests de diagnostic mondiaux.
Cette veille permanente est la seule façon d’éviter d’être pris de court par une épidémie.
L’étude du résistome : cartographier tout le potentiel de résistance
Connaissez-vous le concept de « résistome » ? Il désigne l’intégralité des gènes de résistance présents dans un échantillon donné, qu’il s’agisse du microbiote intestinal d’un patient ou d’un environnement hospitalier spécifique.
Grâce au séquençage à haut débit, nous pouvons désormais cartographier cet arsenal génétique invisible. L’idée est de prédire les risques infectieux bien avant qu’une pathologie ne se déclare chez le patient.
Ce domaine de recherche actif prépare une médecine plus préventive et personnalisée.
L’enjeu de l’accessibilité : des tests pour tous, partout
Si les technologies de pointe impressionnent, elles restent coûteuses et complexes à déployer. L’urgence actuelle est de concevoir des tests rapides, fiables et abordables pour les pays disposant de ressources limitées.
Le programme BIRDY de l’Institut Pasteur illustre cette volonté d’adapter les diagnostics. Cette initiative surveille la résistance chez les nouveau-nés dans les zones vulnérables pour ajuster les prises en charge.
L’antibiorésistance est mondiale ; le diagnostic doit l’être pour garantir une hygiène rigoureuse.
L’identification des bactéries résistantes exige une alliance rigoureuse entre la précision de la culture classique et la rapidité de la biologie moléculaire. Cette complémentarité garantit un diagnostic fiable, indispensable pour adapter les traitements et freiner la transmission. L’avenir repose désormais sur l’accessibilité de ces technologies pour une lutte mondiale efficace.
FAQ
Comment détermine-t-on la résistance d’une bactérie aux antibiotiques ?
La méthode de référence pour évaluer la sensibilité d’une bactérie est l’antibiogramme. Cette technique consiste à mettre la bactérie en culture en présence de différents antibiotiques. On observe ensuite si la croissance bactérienne est stoppée ou si elle se poursuit malgré le traitement. Une *absence d’inhibition indique clairement que la bactérie est résistante*.
En complément, les laboratoires utilisent désormais des méthodes moléculaires comme la PCR. Au lieu d’attendre la croissance de la bactérie, ces tests recherchent directement la présence de gènes de résistance spécifiques dans son ADN. Cette approche permet d’obtenir une réponse en quelques heures seulement.
Quelles techniques permettent d’identifier une bactérie en laboratoire ?
L’identification bactérienne moderne repose majoritairement sur la spectrométrie de masse MALDI-TOF. Cette technologie de pointe analyse le profil des protéines de la bactérie et le compare à une base de données. Elle permet d’identifier l’espèce précise en quelques minutes à partir d’une colonie isolée.
Les méthodes biochimiques classiques restent également utilisées. Elles consistent à observer le métabolisme de la bactérie, par exemple sa capacité à consommer certains sucres ou à produire des enzymes spécifiques. Ces tests dressent une « « carte d’identité » métabolique unique pour chaque espèce.
Comment observe-t-on les bactéries avant de tester leur résistance ?
L’observation initiale s’effectue au microscope optique, généralement après une coloration de Gram. Cette étape fondamentale permet de visualiser la forme des bactéries (coques ou bacilles) et de les classer en deux grandes catégories : Gram positif ou Gram négatif. Cette distinction oriente immédiatement les premières décisions médicales.
Cette observation microscopique est un prérequis indispensable. Elle valide la présence de bactéries dans le prélèvement et guide le choix des milieux de culture sur lesquels on effectuera ensuite les tests d’identification et de résistance plus poussés.
Quelles sont les principales méthodes pour classifier et identifier les pathogènes ?
On distingue trois approches complémentaires pour classer et identifier les bactéries. L’approche phénotypique observe les caractéristiques visibles et le comportement métabolique du germe. L’approche protéomique, via le MALDI-TOF, identifie la bactérie grâce à la masse de ses protéines.
Enfin, l’approche génotypique analyse le matériel génétique (ADN) de la bactérie. C’est la méthode la plus précise, car elle permet non seulement d’identifier l’espèce, mais aussi de détecter les mutations responsables de la résistance aux antibiotiques.



